연세소식
-
[연구 프론티어] 조진원 교수팀, 암세포의 무한증식을 가능하게 하는 당수식화 기작 규명
연세대학교 홍보팀 / news@yonsei.ac.kr2020-06-30 -
조진원 교수팀, 암세포의 무한증식을 가능하게 하는 당수식화 기작 규명
'오글루넥' 당분자 제어로 암에 효과적인 대응 가능케 해

조진원 교수(시스템생물학) 연구팀은 종양억제단백질 LATS2의 오글루넥수식화를 최초로 발견하고 이러한 당수식화 현상이 암세포의 무한증식을 가능하게 한다는 사실을 규명했다. 연구결과는 세계적인 학술지 Proceedings of the National Academy of Sciences of the United States of America(PNAS:미국국립과학원회보)에 게재됐다(제1저자: 김은아 박사).

우리 몸의 세포는 이웃한 세포의 수가 증가해 세포밀도가 높아지면 증식을 멈춘다. 간, 폐 등의 조직이 적절한 크기를 유지할 수 있는 것은 바로 이러한 조절 덕분이다. 그러나 암세포는 세포가 과밀한 환경에서도 지속적으로 그 수를 늘려간다. 암세포가 무한증식이 가능한 것은 세포의 증식을 조절하는 ‘히포신호전달(Hippo signaling pathway)’이 원활하게 일어나지 않기 때문이다.
조진원 교수팀은 히포신호전달의 중심인자인 종양억제단백질 'LATS2'에 당분자의 일종인 오글루넥(O-GlcNAc)이 달라붙으면 LATS2의 활성이 억제돼 히포신호전달을 지속적으로 방해한다는 사실을 밝혔다.
암세포는 정상세포보다 훨씬 많은 포도당을 흡수한다. 따라서 포도당을 원료로 하는 오글루넥수식화의 비정상적인 증가는 여러 암세포에서 관찰되는 공통적인 현상이다. 연구팀은 이러한 암세포 내의 비정상적으로 증가된 오글루넥수식화를 억제시켰을 때, 히포신호전달의 최종 단백질인 전사인자 YAP/TAZ가 핵 밖으로 이동하는 것을 확인했다(그림1).
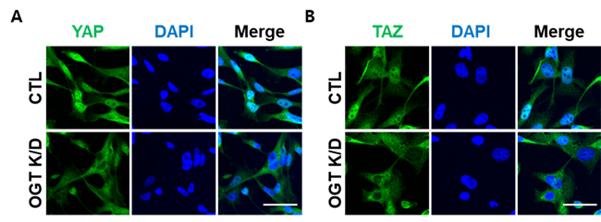
[그림 1 : 오글루넥전이효소(OGT)를 감소시켜 오글루넥수식화를 줄였을 때 YAP(A)과 TAZ(B)의 위치 변화]
YAP/TAZ의 직접적인 억제자인 LATS2의 오글루넥수식화를 조사한 결과, LATS2의 특정 아미노산 잔기(436번째 아미노산인 트레오닌)에 부착된 오글루넥이 LATS2의 활성화에 관여하는 MOB1단백질과의 결합을 억제해 LATS2의 활성화를 막았다. 실제로 그 자리에 오글루넥이 붙지 않는 LATS2 돌연변이의 경우 LATS2의 활성이 증가해 종양의 성장을 반 이상 감소시켰다(그림2).
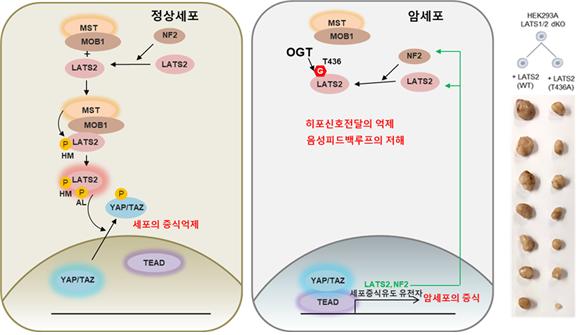
[그림 2 : LATS2의 오글루넥수식화에 의한 히포신호전달 저해에 따른 종양성장 촉진 모델]
LATS2는 YAP/TAZ의 직접적인 저해자이기도 하지만 YAP/TAZ가 발현시키는 단백질이기도 하다. 즉, LATS2는 YAP/TAZ의 활성을 일정수준으로 지속시켜주는 음성피드백의 핵심단백질인 셈이다. 따라서 조진원 교수팀의 연구결과는 암세포에서 히포신호전달이 지속적으로 약화되는 이유를 설명할 수 있다는 점에서 그 의의가 크다.
현대의학의 지속적인 발달에도 불구하고 암에 의한 사망률은 매년 증가하고 있다. 오글루넥의 비정상적인 증가와 히포신호전달의 약화는 다양한 기원의 여러 암세포에서 공통적으로 나타나는 형질이며, 히포신호전달은 암의 증식뿐 아니라 전이 및 발생과도 깊게 연관되어 있다. 따라서 LATS2에 붙는 '오글루넥' 당분자를 제어할 수 있다면 오랜 시간 동안 인류를 위협해 온 암에 효과적으로 대응할 수 있을 것이라는 ‘달콤한’ 기대를 해본다.
본 연구는 과학기술정보통신부와 한국연구재단이 추진하는 집단연구지원사업 및 바이오·의료기술개발사업의 지원으로 수행됐다.

논문주소
https://doi.org/10.1073/pnas.1913469117
논문명
O-GlcNAcylation on LATS2 disrupts the Hippo pathway by inhibiting its activity (2020년 6월 발간, 2018년 IF=9.58)
저자 정보
조진원(교신저자, 연세대 시스템생물학과, 융합오믹스 의생명과학 협동과정, 당수식화네트워크센터, 김은아(제1저자, 연세대 당수식화네트워크센터)외 12명의 공동저자
연구결과의 요약
암세포 내의 LATS2는 세포 안으로 흡수된 과량의 포도당과 OGT의 증가로 오글루넥이 붙게 된다. 오글루넥의 부착은 LATS2와 MST를 연결시켜주는 MOB1단백질의 결합을 방해한다. MST는 LATS2를 인산화시켜 활성을 유도하는 히포신호전달의 구성단백질이다. 따라서 LATS2는 MST에 의해 인산화되지 않아 활성화되지 못한다. 그 결과 YAP과 TAZ는 LATS2에 의해 인산화되지 못해 핵 안에 많이 존재하게 된다. 전사인자인 YAP과 TAZ는 각각 TEAD와 결합하여 TEAD에 의한 유전자 발현을 증가시킨다. 이 때 발현이 증가되는 유전자는 세포증식에 관여하는 단백질 및 LATS2, NF2의 유전자이다. NF2는 LATS2를 MST-MOB복합체로 이동시켜 주는 단백질이다. 정상세포의 경우 이러한 LATS2와 NF2의 증가가 다시금 YAP과 TAZ의 활성을 약화시켜 과도한 세포 증식의 지속을 막는다. 하지만 암세포의 경우 LATS2에 부착된 오글루넥에 의해 LATS2의 활성이 억제되므로 이러한 음성피드백에 의한 효과가 저해되고 결과적으로 히포신호절달이 지속적으로 약화되어 무한증식을 할 수 있다.
용 어 설 명
1. 오글루넥수식화(O-GlcNAc modification)
오글루넥은 포도당을 원료로 하는 단일 당분자이다. 세포 내의 약 3-5%의 포도당은 오글루넥을 합성하는데 사용된다. 오글루넥은 오글루넥전이효소인 OGT에 의해 타겟단백질의 세린 트레오닌 잔기에 붙게 되고, OGA 단백질에 의해 타겟단백질에서 떨어지게 된다. 단백질의 세린 트레오닌 잔기는 인산화가 일어나는 자리이기도 하다. 세포 내에서 일어나는 인산화 반응은 다양한 신호전달기작에 관여한다. 따라서 오글루넥수식화는 인산화로 매개되는 다양한 신호전달에 영향을 미칠 수 있다. 오글루넥수식화는 암 뿐 아니라 치매, 당뇨 등 여러 질환에도 깊숙이 관여되어 있다.
2. 히포신호전달경로(Hippo signaling pathway)
히포신호전달경로는 세포의 증식을 억제하고 사멸(apoptosis) 유도하는 세포 내 신호전달 경로이다. 히포신호전달을 작동시키는 대표적인 자극은 세포간의 접촉이다. 따라서 세포로 과밀한 환경에서 히포신호전달이 일어나 세포의 증식이 억제되고 세포사멸이 유도되어 일정 수준의 세포 밀도를 유지할 수 있다. 히포신호전달경로는 세린/트레오닌 키나아제인 MST1/2, LATS1/2 그리고 최종단백질인 전사인자 YAP/TAZ로 이루어져 있다. MST1/2는 하위 단백질인 LATS1/2에 인산기를 붙여 활성화시킨다. 이때 MST1/2와 LATS1/2를 연결시켜 주는 단백질은 MOB1이며, MST1-MOB1 복합체로 LATS2를 이동시켜 주는 역할은 NF2가 수행한다. LATS1/2 역시 YAP과 TAZ에 인산기를 직접적으로 부착하여 YAP과 TAZ가 세포질에 위치하게 할 뿐 아니라 분해를 유도하여 핵 내의 YAP과 TAZ의 양을 줄인다. YAP과 TAZ는 핵 내의 TEAD단백질을 도와 세포증식을 촉진하고 세포사멸을 억제하는 유전자 발현을 유도한다. 따라서 히포신호전달이 작동하면 세포분열이 저해되고 사멸이 촉진된다. 히포신호전달은 암의 증식뿐 아니라 암의 전이 및 암의 발생에도 관여한다.
히포신호전달경로의 음성 피드백: 활성화된 YAP과 TAZ는 LATS2와 NF2의 유전자 발현을 유도한다. 즉 활성이 과도하게 증가한 YAP과 TAZ는 활성화된 LATS2의 양을 늘려 자신들의 활성을 억제한다.
- vol. 전체
- vol. 635
- vol. 634
- vol. 633
- vol. 632
- vol. 631
- vol. 630
- vol. 629
- vol. 628
- vol. 627
- vol. 626
- vol. 625
- vol. 624
- vol. 623
- vol. 622
- vol. 621
- vol. 620
- vol. 619
- vol. 618
- vol. 617
- vol. 616
- vol. 615
- vol. 614
- vol. 613
- vol. 612
- vol. 611
- vol. 610
- vol. 609
- vol. 608
- vol. 607
- vol. 606
- vol. 605
- vol. 604
- vol. 603
- vol. 602
- vol. 601
- vol. 600
- vol. 599
- vol. 598
- vol. 597
- vol. 596
- vol. 595
- vol. 594
- vol. 593
- vol. 592
- vol. 591
- vol. 590
- vol. 589
- vol. 587
- vol. 586
- vol. 585
- vol. 584
- vol. 583
- vol. 582
- vol. 581
- vol. 580
- vol. 579
- vol. 578
- vol. 577
- vol. 576
- vol. 575
- vol. 574
- vol. 573
- vol. 572
- vol. 571
- vol. 570
- vol. 569
- vol. 568
- vol. 567
- vol. 566
- vol. 565
- vol. 564
- vol. 563
- vol. 562
- vol. 561
- vol. 560
- vol. 559
- vol. 558
- vol. 557
- vol. 556
- vol. 555
- vol. 554
- vol. 553
- vol. 552
- vol. 551
- vol. 550
- vol. 549
- vol. 548
- vol. 547
- vol. 546
- vol. 545
- vol. 544
- vol. 543
- vol. 542
- vol. 541
- vol. 540
- vol. 539
- vol. 538
- vol. 537
- vol. 536
- vol. 535
- vol. 534
- vol. 533
- vol. 532
- vol. 531
- vol. 530
- vol. 529
- vol. 528
- vol. 527
- vol. 526
- vol. 525
- vol. 524
- vol. 523
- vol. 522
- vol. 521
- vol. 520
- vol. 519
- vol. 518
- vol. 517
- vol. 516
- vol. 515
- vol. 514
- vol. 513
- vol. 512
- vol. 511
- vol. 510
- vol. 509
- vol. 508
- vol. 507
- vol. 506
- vol. 505
- vol. 504
- vol. 503
- vol. 502
- vol. 501
- vol. 500
- vol. 499
- vol. 498
- vol. 497
- vol. 496
- vol. 495
- vol. 494
- vol. 493
- vol. 492
- vol. 491
- vol. 490
- vol. 489
- vol. 488
- vol. 487
- vol. 486
- vol. 485
- vol. 484
- vol. 483
- vol. 482
- vol. 481
- vol. 480
- vol. 479
- vol. 478
- vol. 477
- vol. 476
- vol. 475
- vol. 474
- vol. 473
- vol. 472
- vol. 471
- vol. 470
- vol. 469
- vol. 468
- vol. 467
- vol. 466
- vol. 465
- vol. 464
- vol. 463
- vol. 462
- vol. 461
- vol. 460
- vol. 459
- vol. 458
- vol. 457
- vol. 456
- vol. 455
- vol. 454
- vol. 453
- vol. 452
- vol. 451
- vol. 450
- vol. 449
- vol. 448
- vol. 447
- vol. 446
- vol. 445
- vol. 444
- vol. 443
- vol. 442
- vol. 441
- vol. 440
- vol. 439
- vol. 438
- vol. 437
- vol. 436
- vol. 435
- vol. 434
- vol. 433
- vol. 432
- vol. 431
- vol. 430
- vol. 429
- vol. 428
- vol. 427
- vol. 426
- vol. 425
- vol. 424
- vol. 423
- vol. 422
- vol. 421
- vol. 420
- vol. 419
- vol. 418
- vol. 417
- vol. 416
- vol. 415
- vol. 414
- vol. 413
- vol. 412
- vol. 411
- vol. 410
- vol. 409
- vol. 408
- vol. 407
- vol. 406
- vol. 405
- vol. 404
- vol. 403
- vol. 402
- vol. 401
- vol. 400
- vol. 399
- vol. 398
- vol. 397
- vol. 396
- vol. 395
- vol. 394
- vol. 393
- vol. 392
- vol. 391
- vol. 390
- vol. 389
- vol. 388
- vol. 387
- vol. 386
- vol. 385
- vol. 384
- vol. 383
- vol. 382
- vol. 381
- vol. 380
- vol. 379
- vol. 378
- vol. 377
- vol. 376
- vol. 375
- vol. 374
- vol. 373
- vol. 372
- vol. 371
- vol. 370
- vol. 369
- vol. 368
- vol. 367
- vol. 366
- vol. 365
- vol. 364
- vol. 363
- vol. 362
- vol. 361
- vol. 360
- vol. 359
- vol. 358
- vol. 357
- vol. 356
- vol. 355
- vol. 354
- vol. 353
- vol. 352
- vol. 351
- vol. 350
- vol. 349
- vol. 348
- vol. 347
- vol. 346
- vol. 345
- vol. 344
- vol. 343
- vol. 342
- vol. 341
- vol. 340
- vol. 339
- vol. 338
- vol. 337
- vol. 336
- vol. 335
- vol. 334
- vol. 333
- vol. 332
- vol. 331
- vol. 330
- vol. 329
- vol. 328
- vol. 327
- vol. 326
- vol. 325
- vol. 324
- vol. 323
- vol. 322
- vol. 321
- vol. 320
- vol. 319
- vol. 318
- vol. 317
- vol. 316
- vol. 315
- vol. 314
- vol. 313
- vol. 312
- vol. 311
- vol. 310
- vol. 309
- vol. 308
- vol. 307
- vol. 306
- vol. 305
- vol. 304
- vol. 303
- vol. 302
- vol. 301
- vol. 300
- vol. 299
- vol. 298
- vol. 297
- vol. 296
- vol. 295
- vol. 294
- vol. 293
- vol. 292
- vol. 291
- vol. 290
- vol. 289
- vol. 288
- vol. 287
- vol. 286
- vol. 285
- vol. 284
- vol. 283
- vol. 282
- vol. 281
- vol. 280
- vol. 279
- vol. 278
- vol. 277
- vol. 276
- vol. 275
- vol. 274
- vol. 273
- vol. 272
- vol. 271
- vol. 270
- vol. 269
- vol. 268
- vol. 267
- vol. 266
- vol. 265
- vol. 264
- vol. 263
- vol. 262
- vol. 261
- vol. 260
- vol. 259
- vol. 258
- vol. 257
- vol. 256
- vol. 255
- vol. 254
- vol. 253
- vol. 252
- vol. 251
- vol. 250
- vol. 249
- vol. 248
- vol. 247
- vol. 246
- vol. 245
- vol. 244
- vol. 243
- vol. 242
- vol. 241
- vol. 240
- vol. 239
- vol. 238
- vol. 237
- vol. 236
- vol. 235
- vol. 234
- vol. 233
- vol. 232
- vol. 231
- vol. 230
- vol. 229
- vol. 228
- vol. 227
- vol. 226
- vol. 225
- vol. 224
- vol. 223
- vol. 222
- vol. 221
- vol. 220
- vol. 219
- vol. 218
- vol. 217
- vol. 216
- vol. 215
- vol. 214
- vol. 213
- vol. 212
- vol. 211
- vol. 210
- vol. 209
- vol. 208
- vol. 207
- vol. 206
- vol. 205
- vol. 204
- vol. 203
- vol. 202
- vol. 201
- vol. 189
- vol. 188
- vol. 187
- vol. 186
- vol. 185
- vol. 184
- vol. 183
- vol. 182
- vol. 181
- vol. 180
- vol. 179
- vol. 178
- vol. 177
- vol. 176
- vol. 175
- vol. 174
- vol. 173
- vol. 172
- vol. 171
- vol. 170
- vol. 169
- vol. 168
- vol. 167
- vol. 166
- vol. 165
- vol. 164
- vol. 163
- vol. 162
- vol. 161
- vol. 160
- vol. 159
- vol. 158
- vol. 157
- vol. 156
- vol. 155
- vol. 154
- vol. 153
- vol. 152
- vol. 151
연세소식 신청방법
아래 신청서를 작성 후 news@yonsei.ac.kr로 보내주세요신청서 다운로드