연세소식
-
[연구 프론티어] 송재환 교수팀, 새로운 암 질환 치료 가능성 열어
연세대학교 홍보팀 / news@yonsei.ac.kr2016-03-05 -
송재환 교수팀, 새로운 암 질환 치료 가능성 열어
세포사멸 기작인 네크롭토시스를 억제하는 주요 인자 발굴
‘네이처 셀 바이올로지’에 논문 발표

생화학과 송재환 교수팀(공동 제1저자 서진호 박사과정, 이은우 박사후연구원)은 세포사멸 기작인 네크롭토시스 주요 단백질(RIPK1와 RIPK3)의 양을 조절하는 단백질을 동정(CHIP)해, 이를 유전자 변형 동물 모델에 적용함으로써 동정한 단백질이 네크롭토시스 작용에 있어서 중요한 인자임을 밝혔다. 이번 연구는 벨기에 겐트대학의 피터 반데나베엘(Peter Vandenabeele) 교수팀, 서울대 성제경 교수팀 및 KIST 이철주 교수팀과의 협력연구를 통해 이뤄졌다.
세포사멸 기작은 개체의 항상성을 유지하는 데 매우 중요하다. 이러한 기작에 오작동이 일어나면 암, 자가면역질환, 감염성 질환 등의 많은 질환이 일어나는 것으로 알려져 있으며, 세포사멸 기작은 아팝토시스라는 세포자살 기작을 비롯해 여러 종류의 형태로 진행된다.
최근 세포사멸 및 광범위한 면역반응을 일으키는 새로운 기작 네크롭토시스가 규명되고 있다. 이는 기존의 세포괴사로 알려진 네크로시스와 비슷한 형태다. 그러나 세포가 죽게 되지만 그러한 과정이 외부 물리적 자극에 의해 수동적으로 일어나는 네크로시스와 달리 네크롭토시스는 세포 내 신호 전달 체계를 통해 조절되는 새로운 형태의 능동적 세포사멸 기작으로 보고되고 있다.
네크롭토시스는 아팝토시스를 회피하는 기작을 가진 바이러스나 박테리아에 의한 감염상황에서 면역세포가 개체를 보호하기 위해 분비하는 사이토카인에 의해 주로 유도된다. 네크롭토시스에 의한 세포사멸 시 발생하는 세포의 부산물을 면역세포가 다시 이용해 근처 감염된 세포들을 광범위하게 제거하는 기작으로 알려져 있다. 실제로 많은 연구들을 통해 저산소증 상황에서 일어나는 세포사멸기작, 사이토카인 폭풍(패혈증)에 의한 광범위한 세포사멸, 다양한 면역관련 질환 등에서 네크롭토시스의 중요성이 증명되고 있다. 또한 네크롭토시스를 조절할 수 있는 핵심 인자를 발견하고 그 조절 기작을 이해하는 다양한 연구가 전 세계적으로 진행 중에 있다. 그러나 아직까지는 제대로 된 조절 인자가 발견되지 않고 있으며 이 때문에 네크롭토시스 기작에 대한 기초적 이해 및 이를 이용한 치료 방안에 어려움이 많다.
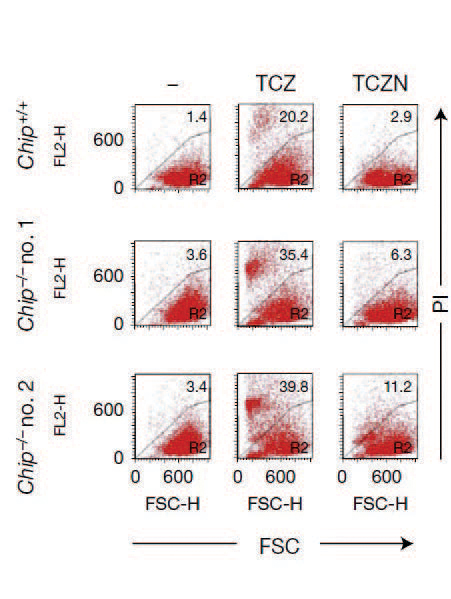
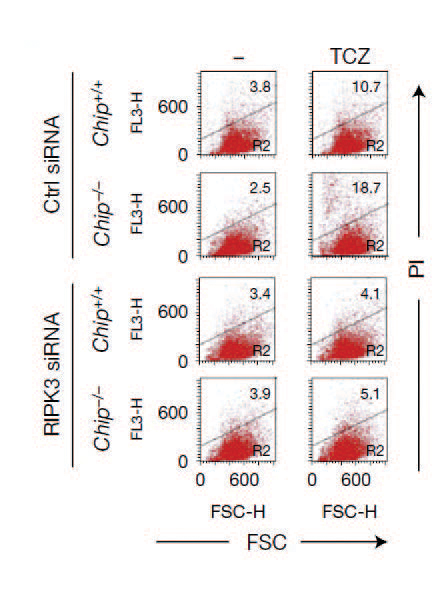
그림 1 CHIP 및 RIPK3 단백질이 결손된 세포를 이용한 네크롭토시스 실험
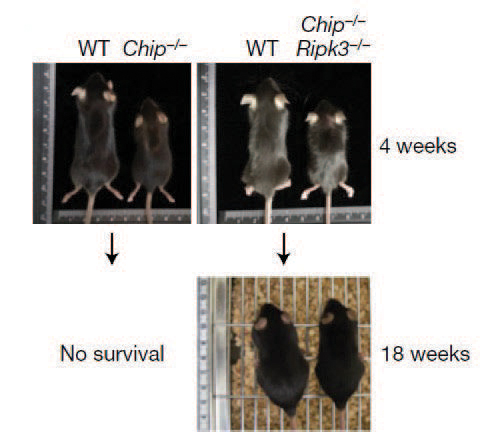
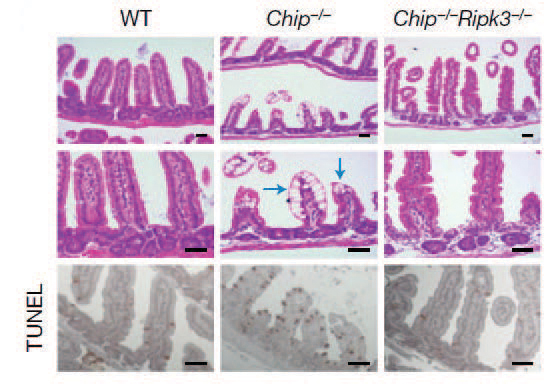
그림 2 CHIP 및 RIPK3 단백질이 결손 된 유전자 변형 쥐 분석
송재환 교수 연구팀은 네크롭토시스에서 가장 핵심적인 역할을 하는 RIPK3 단백질의 유비퀴틴화에 관심을 가지고 연구를 수행했다. 세포의 항상성 및 다양한 세포신호전달체계에 관여하는 유비퀴틴화 부착 단백질인 CHIP이 없는 배아섬 유아세포(mouse embryonic fibroblast, MEF)의 경우 네크롭토시스 자극에 반응해 더 빠르게 세포사멸이 일어나는 것을 확인했다. 나아가 이 같은 세포는 정상세포에 비해 네크롭토시스 주요인자인 RIPK1과 RIPK3 단백질의 양이 매우 증가해 있는 것을 밝혀냈다. 또한 이러한 민감성은 네크롭토시스 주요인자인 RIPK3를 같이 없앴을 경우, CHIP의 결손에 의한 효과가 감소하는 것을 확인 할 수 있었다(그림 1).
연구진은 이를 동물 모델에서 확인하기 위해 CHIP, RIPK3가 결손된 유전자 변형 쥐를 이용해 실험을 수행했다. CHIP이 결손된 유전자 변형 쥐는 매우 작고, 두 달을 채 살지 못했다. 반면, RIPK3가 동시에 결손된 유전자 변형 쥐는 두 달 이상 생존이 가능하며, 처음에는 크기가 작지만 이후 일반적인 쥐와 크게 차이가 없는 상태가 됐다. 실제로 CHIP이 결손된 유전자 변형 쥐의 경우 네크롭토시스의 표현형인 소장의 융털들이 무너져 있는 것을 확인했으며, 이러한 표현형은 RIPK3를 함께 결손시킨 유전자 변형 쥐에서는 발견되지 않았다(그림 2).
위 결과를 통해 송재환 교수 연구팀은 CHIP 단백질이 네크롭토시스의 주요 억제 인자임을 분자생물학적, 병리학적 측면에서 규명했다. 향후 본 연구결과를 이용해 암, 자가면역 질환, 바이러스 및 박테리아 감염에 따른 패혈증 등을 치료하는 새로운 방법에 기여할 수 있을 것으로 예상된다.
이번 연구는 미래창조과학부와 한국연구재단의 리더연구자사업 및 교육부와 한국연구재단의 대통령 포스트닥(Post-Doc) 펠로우십 지원을 받아 진행됐다. 한편 연구결과는 ‘네이처 셀 바이올로지(Nature Cell Biology)’ 온라인판 2월 23일자에 게재됐다.
- vol. 전체
- vol. 635
- vol. 634
- vol. 633
- vol. 632
- vol. 631
- vol. 630
- vol. 629
- vol. 628
- vol. 627
- vol. 626
- vol. 625
- vol. 624
- vol. 623
- vol. 622
- vol. 621
- vol. 620
- vol. 619
- vol. 618
- vol. 617
- vol. 616
- vol. 615
- vol. 614
- vol. 613
- vol. 612
- vol. 611
- vol. 610
- vol. 609
- vol. 608
- vol. 607
- vol. 606
- vol. 605
- vol. 604
- vol. 603
- vol. 602
- vol. 601
- vol. 600
- vol. 599
- vol. 598
- vol. 597
- vol. 596
- vol. 595
- vol. 594
- vol. 593
- vol. 592
- vol. 591
- vol. 590
- vol. 589
- vol. 587
- vol. 586
- vol. 585
- vol. 584
- vol. 583
- vol. 582
- vol. 581
- vol. 580
- vol. 579
- vol. 578
- vol. 577
- vol. 576
- vol. 575
- vol. 574
- vol. 573
- vol. 572
- vol. 571
- vol. 570
- vol. 569
- vol. 568
- vol. 567
- vol. 566
- vol. 565
- vol. 564
- vol. 563
- vol. 562
- vol. 561
- vol. 560
- vol. 559
- vol. 558
- vol. 557
- vol. 556
- vol. 555
- vol. 554
- vol. 553
- vol. 552
- vol. 551
- vol. 550
- vol. 549
- vol. 548
- vol. 547
- vol. 546
- vol. 545
- vol. 544
- vol. 543
- vol. 542
- vol. 541
- vol. 540
- vol. 539
- vol. 538
- vol. 537
- vol. 536
- vol. 535
- vol. 534
- vol. 533
- vol. 532
- vol. 531
- vol. 530
- vol. 529
- vol. 528
- vol. 527
- vol. 526
- vol. 525
- vol. 524
- vol. 523
- vol. 522
- vol. 521
- vol. 520
- vol. 519
- vol. 518
- vol. 517
- vol. 516
- vol. 515
- vol. 514
- vol. 513
- vol. 512
- vol. 511
- vol. 510
- vol. 509
- vol. 508
- vol. 507
- vol. 506
- vol. 505
- vol. 504
- vol. 503
- vol. 502
- vol. 501
- vol. 500
- vol. 499
- vol. 498
- vol. 497
- vol. 496
- vol. 495
- vol. 494
- vol. 493
- vol. 492
- vol. 491
- vol. 490
- vol. 489
- vol. 488
- vol. 487
- vol. 486
- vol. 485
- vol. 484
- vol. 483
- vol. 482
- vol. 481
- vol. 480
- vol. 479
- vol. 478
- vol. 477
- vol. 476
- vol. 475
- vol. 474
- vol. 473
- vol. 472
- vol. 471
- vol. 470
- vol. 469
- vol. 468
- vol. 467
- vol. 466
- vol. 465
- vol. 464
- vol. 463
- vol. 462
- vol. 461
- vol. 460
- vol. 459
- vol. 458
- vol. 457
- vol. 456
- vol. 455
- vol. 454
- vol. 453
- vol. 452
- vol. 451
- vol. 450
- vol. 449
- vol. 448
- vol. 447
- vol. 446
- vol. 445
- vol. 444
- vol. 443
- vol. 442
- vol. 441
- vol. 440
- vol. 439
- vol. 438
- vol. 437
- vol. 436
- vol. 435
- vol. 434
- vol. 433
- vol. 432
- vol. 431
- vol. 430
- vol. 429
- vol. 428
- vol. 427
- vol. 426
- vol. 425
- vol. 424
- vol. 423
- vol. 422
- vol. 421
- vol. 420
- vol. 419
- vol. 418
- vol. 417
- vol. 416
- vol. 415
- vol. 414
- vol. 413
- vol. 412
- vol. 411
- vol. 410
- vol. 409
- vol. 408
- vol. 407
- vol. 406
- vol. 405
- vol. 404
- vol. 403
- vol. 402
- vol. 401
- vol. 400
- vol. 399
- vol. 398
- vol. 397
- vol. 396
- vol. 395
- vol. 394
- vol. 393
- vol. 392
- vol. 391
- vol. 390
- vol. 389
- vol. 388
- vol. 387
- vol. 386
- vol. 385
- vol. 384
- vol. 383
- vol. 382
- vol. 381
- vol. 380
- vol. 379
- vol. 378
- vol. 377
- vol. 376
- vol. 375
- vol. 374
- vol. 373
- vol. 372
- vol. 371
- vol. 370
- vol. 369
- vol. 368
- vol. 367
- vol. 366
- vol. 365
- vol. 364
- vol. 363
- vol. 362
- vol. 361
- vol. 360
- vol. 359
- vol. 358
- vol. 357
- vol. 356
- vol. 355
- vol. 354
- vol. 353
- vol. 352
- vol. 351
- vol. 350
- vol. 349
- vol. 348
- vol. 347
- vol. 346
- vol. 345
- vol. 344
- vol. 343
- vol. 342
- vol. 341
- vol. 340
- vol. 339
- vol. 338
- vol. 337
- vol. 336
- vol. 335
- vol. 334
- vol. 333
- vol. 332
- vol. 331
- vol. 330
- vol. 329
- vol. 328
- vol. 327
- vol. 326
- vol. 325
- vol. 324
- vol. 323
- vol. 322
- vol. 321
- vol. 320
- vol. 319
- vol. 318
- vol. 317
- vol. 316
- vol. 315
- vol. 314
- vol. 313
- vol. 312
- vol. 311
- vol. 310
- vol. 309
- vol. 308
- vol. 307
- vol. 306
- vol. 305
- vol. 304
- vol. 303
- vol. 302
- vol. 301
- vol. 300
- vol. 299
- vol. 298
- vol. 297
- vol. 296
- vol. 295
- vol. 294
- vol. 293
- vol. 292
- vol. 291
- vol. 290
- vol. 289
- vol. 288
- vol. 287
- vol. 286
- vol. 285
- vol. 284
- vol. 283
- vol. 282
- vol. 281
- vol. 280
- vol. 279
- vol. 278
- vol. 277
- vol. 276
- vol. 275
- vol. 274
- vol. 273
- vol. 272
- vol. 271
- vol. 270
- vol. 269
- vol. 268
- vol. 267
- vol. 266
- vol. 265
- vol. 264
- vol. 263
- vol. 262
- vol. 261
- vol. 260
- vol. 259
- vol. 258
- vol. 257
- vol. 256
- vol. 255
- vol. 254
- vol. 253
- vol. 252
- vol. 251
- vol. 250
- vol. 249
- vol. 248
- vol. 247
- vol. 246
- vol. 245
- vol. 244
- vol. 243
- vol. 242
- vol. 241
- vol. 240
- vol. 239
- vol. 238
- vol. 237
- vol. 236
- vol. 235
- vol. 234
- vol. 233
- vol. 232
- vol. 231
- vol. 230
- vol. 229
- vol. 228
- vol. 227
- vol. 226
- vol. 225
- vol. 224
- vol. 223
- vol. 222
- vol. 221
- vol. 220
- vol. 219
- vol. 218
- vol. 217
- vol. 216
- vol. 215
- vol. 214
- vol. 213
- vol. 212
- vol. 211
- vol. 210
- vol. 209
- vol. 208
- vol. 207
- vol. 206
- vol. 205
- vol. 204
- vol. 203
- vol. 202
- vol. 201
- vol. 189
- vol. 188
- vol. 187
- vol. 186
- vol. 185
- vol. 184
- vol. 183
- vol. 182
- vol. 181
- vol. 180
- vol. 179
- vol. 178
- vol. 177
- vol. 176
- vol. 175
- vol. 174
- vol. 173
- vol. 172
- vol. 171
- vol. 170
- vol. 169
- vol. 168
- vol. 167
- vol. 166
- vol. 165
- vol. 164
- vol. 163
- vol. 162
- vol. 161
- vol. 160
- vol. 159
- vol. 158
- vol. 157
- vol. 156
- vol. 155
- vol. 154
- vol. 153
- vol. 152
- vol. 151
- 전체 글 보기
- 연세 뉴스
- 섬김의 리더십
- 여기 연세인
- 화제의 인물
- 연구 프론티어
- 신촌캠퍼스 소식
- 의료원 소식
- 원주캠퍼스 소식
- 국제캠퍼스 소식
- 동정
- 공연 소식
- 교원 보직 발령
- 신임 교원 소개
- 이달의 도서
- 인사 발령
- 지금 SNS에서는
- 캠퍼스 바로알기
- 퇴임 교직원 소개
연세소식 신청방법
아래 신청서를 작성 후 news@yonsei.ac.kr로 보내주세요신청서 다운로드